平衡氧化还原反应
- 氧化数可以用来平衡化学方程
- 方括号之间的罗马数字用来表示牛号。一个原子可以有多种氧化态,例如:
Fe(III) =铁与氧。+3
工作示例:编写整体氧化还原反应

回答
- 步骤1:写出不平衡方程,找出在x中发生变化的原子。

- 步骤2:推导出x,不。变化

- 步骤3:平衡一下,不。变化

- 步骤4:平衡费用
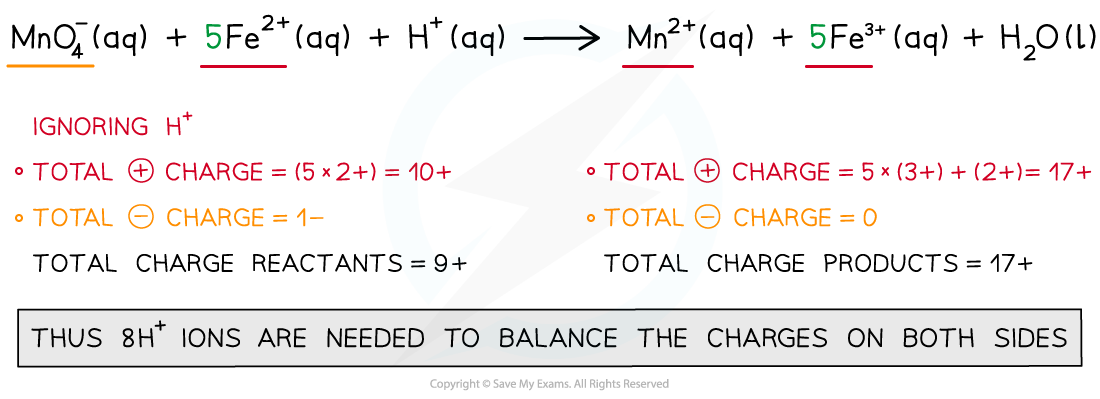
- 步骤5:平衡原子

氧化还原和歧化反应
氧化
- 氧化是获得的氧气,如:
Cu + H2O→CuO + H2
(铜得到一个氧并被氧化)
- 氧化也是失去一个氢,如:
2 nh3.+ 3溴2→N2+ 6哈佛商业评论
(N失去了一个氢被氧化)
- 氧化也是电子的损失,如:
铜2 +→Mg→Mg2 ++铜
(Mg失去了两个电子,被氧化)
- 氧化会导致增加ox, no。,如:
铜2 ++ Mg→Mg2 ++铜
(x的变化。Mg的负能量为+2,因此Mg被氧化)
减少
- 还原法是的损失氧气,如:
铜+ H2O→2CuO + H2
(O已降低)
- 还原法也是一个氢的增益,如:
2 nh3.+ 3溴2→N2+ 6哈佛商业评论
(Br已还原)
- 还原法也是电子的获得,如:
铜2 ++ Mg→Mg2 ++铜
(Cu已被还原)
- 减少导致氧化值降低,如:
铜2 ++ Mg→Mg2 ++铜
(x的变化。Cu的-2,因此Cu被还原)

使用缩写“Oil Rig”来帮助你记住氧化和还原的定义
氧化还原反应
- 氧化还原反应是氧化和还原同时发生的反应
- 在同一反应中,一种物质在氧化,另一种物质在还原,例如:
铜2 ++ Mg→Mg2 ++铜
(Cu已被还原,Mg已被氧化)
示例:氧化和还原

回答
回答1:
氧化:Cl-和x一样,不。增加了1降低:Na+和x一样,不。减少了1
答案2:
氧化的:Mg作为氧。增加了2
降低:铁2 +和x一样,不。减少了2
答案3:
氧化的:获得氧气时的C还原性:当银失去氧气时
歧化反应
- 一个歧化反应一个反应是同一种物质同时被氧化和还原吗

一个不比例反应的例子,在这个反应中,相同的物种(在这种情况下是氯)既被氧化又被还原
工作示例:平衡歧化反应

回答
- 步骤1:写出不平衡方程,找出在x中发生变化的原子。

- 步骤2:推导出x,不。变化

- 步骤3:平衡牛,不。变化

- 步骤4:平衡费用

- 步骤5:平衡原子

